Amino acid and Protein
蛋白质的四级结构
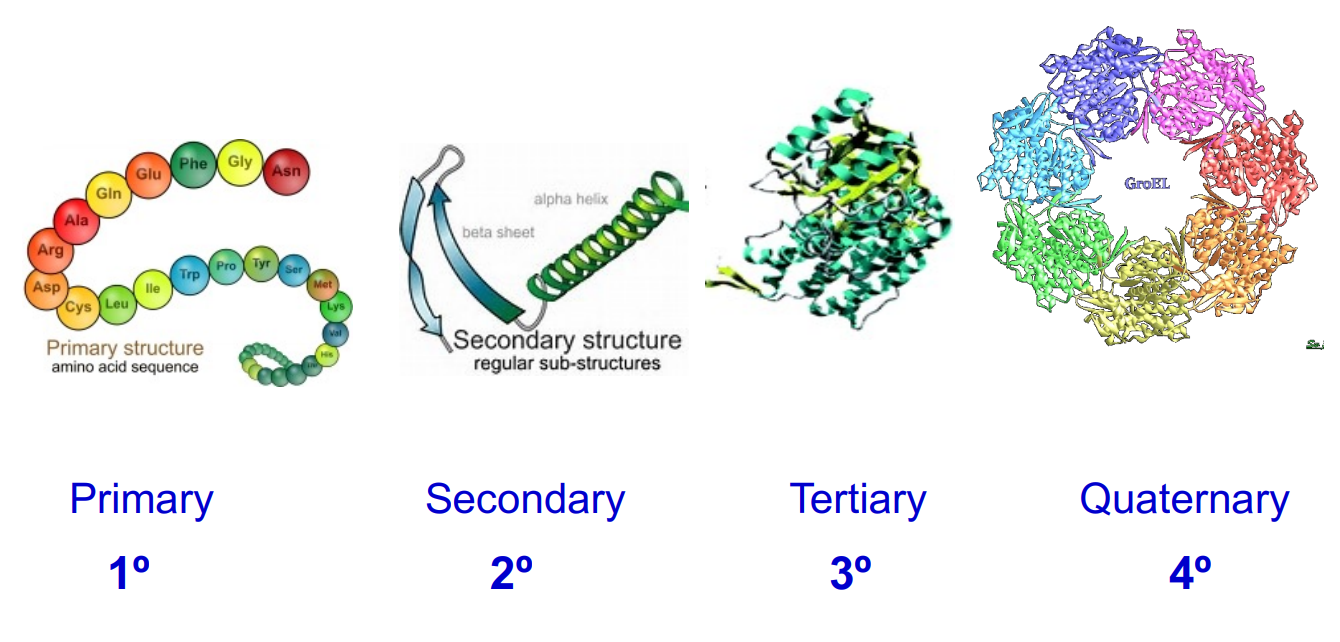
蛋白质是由氨基酸聚合而成的大分子多肽链并折叠形成特定的3D结构。
蛋白质的一级结构:氨基酸的序列
蛋白质的二级结构:多肽链主链骨架本身,在空间上有规律的折叠和盘绕,主要相互作用是氢键;由氨基酸的一级结构决定。
蛋白质的三级结构:是指多肽链在二级结构的基础上进一步盘绕,卷曲,折叠,形成主要通过侧链以次级键以及二硫键维系的完整三维结构。
蛋白质的四级结构:在进行相关作用时,可能存在多个蛋白形成多聚体以发挥功能。(不是所有的蛋白都具备)
由于蛋白质存在这样复杂的四级结构,因此蛋白质具有极高的多样性。
基于功能的蛋白质的分类
- 酶(催化)
- 结构蛋白(角蛋白、胶原蛋白)
- 运输功能(通道蛋白)
- 信息传递(激素,受体)
- 免疫防御(抗体)
- 运动(肌动蛋白,肌球蛋白)
- 储存(豆类种子蛋白)
- ···分子伴侣、荧光蛋白、微管蛋白····
氨基酸的理化性质
#种类
氨基酸一共有22种,其中有两种氨基酸的编码为终止密码子(硒半胱氨酸和吡咯赖氨酸)仅在很少的蛋白中出现。剩余的20种氨基酸中有8种人体无法合成,还有两种合成的量很少,被分别称为必需氨基酸和非必需氨基酸[^1]。
氨基酸的结构
氨基酸顾名思义,
#手性
存在D型和R型两种氨基酸(大多为左手型)
#光学特征
主要吸收280nm的紫外光
#命名和结构

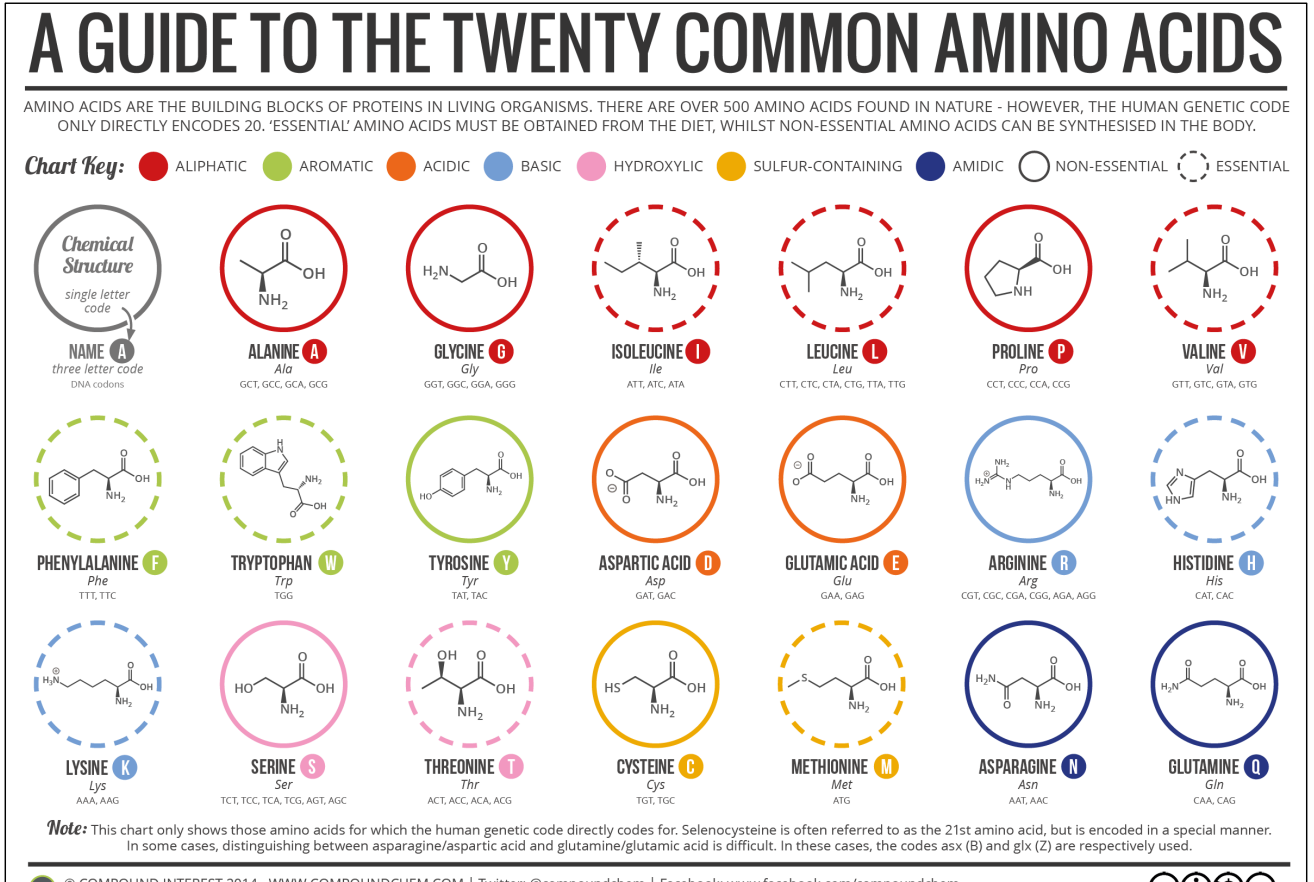
#分类
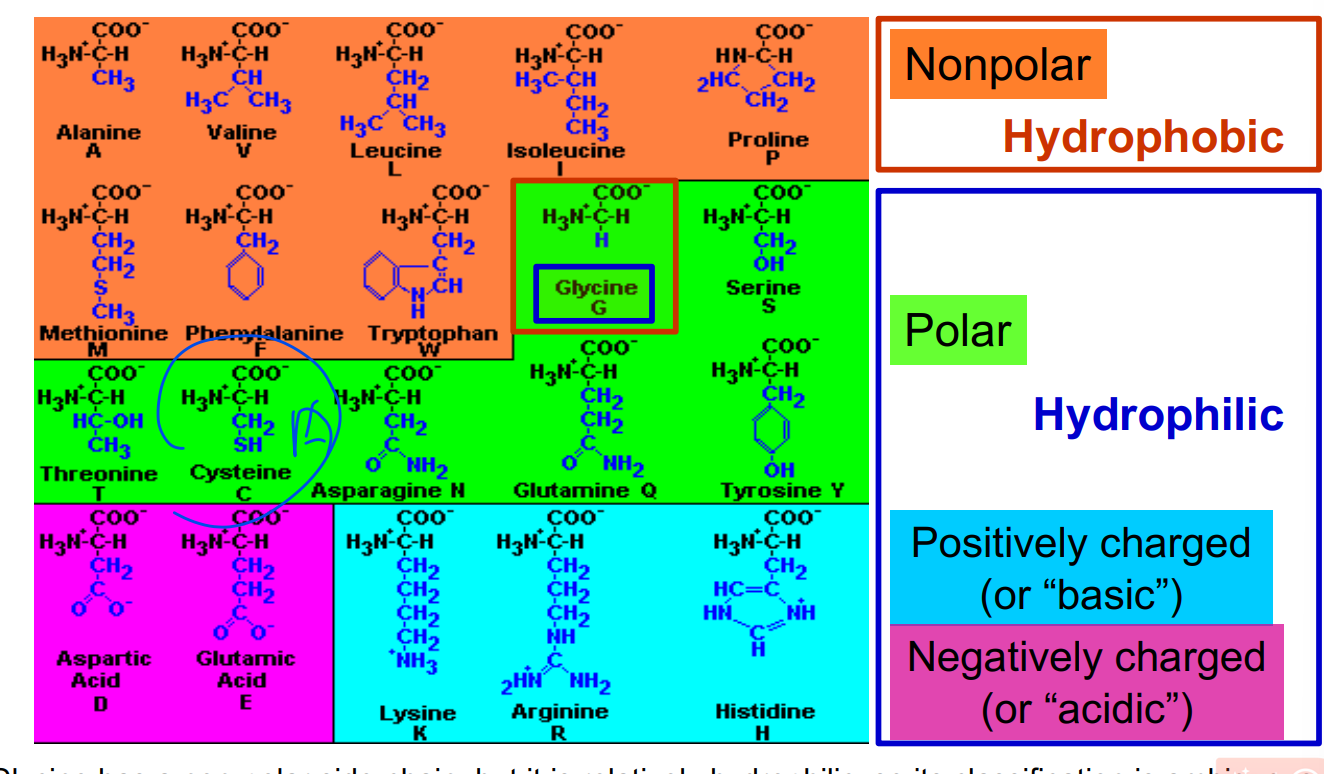
1. 蛋白质氨基酸和非蛋白质氨基酸
- 许多氨基酸具有多种生物学功能,但不参加蛋白质的组成,如:鸟氨酸、瓜氨酸,它们是代谢通路中的中间产物。
2. 亲水氨基酸,疏水氨基酸 :亲水氨基酸的R基团主要带有羟基,巯基,氨基,羧基等亲水基团。
- 亲水指数:氨基酸的亲水指数是描述其支链的亲水性或疏水性的程度大小的的值。亲水指数越大,这种氨基酸的疏水性就越强。
3. 必需氨基酸,非必需氨基酸:甲缬赖异苯亮色苏(组)
4. 亲核氨基酸:即带负电的氨基酸(R基上有羧基:天冬氨酸、谷氨酸);亲电氨基酸:赖、精、组
5. 脂肪类,芳香类:芳香类即带有苯环:苯丙、色、酪
6. 极性,非极性:非极性与熟睡氨基酸一样
7. 人工合成的氨基酸:硒代半胱氨酸
氨基酸的等电点:pl
等电点:使氨基酸静电荷为零时的pH特征点,又称等电pH。即氨基和羧基电离水平相当。[1]
- 对于R基团不会电离(水解)的氨基酸来说等电点就等于:
,pK为基团的酸度系数。 - 对于含有多个可电离(水解)的氨基酸来说情况就较为复杂了,一般采取实验的方式测定:
- 假设将此氨基酸放入pH值极低的环境,写出此时官能团的变化(所有官能团均处于质子化的状态,即得H)
- 假设pH值逐渐升高,模拟出各基团去质子化的状态(pK越低的基团越容易去质子化,即失H)
- 当电荷总和为0时,将前后变化的基团的pK取个平均值,就是所求结果。
比如一个氨基酸含有 -NH2:pK 10.2 -NH2:pK 9.6 -COOH:pK 3.4 三个官能团,求其等电点:
第一步,使溶液处于较低的pH状态,两个氨基都获得一个质子变为-
第二步,向溶液加入氢氧根,使得羧基失去一个质子,此时总电荷为+1
第三步,向溶液加入氢氧根,使pK 值较低的-
若继续添加氢氧根离子,另一个氨基也将失去一个质子,这是总电荷为-1
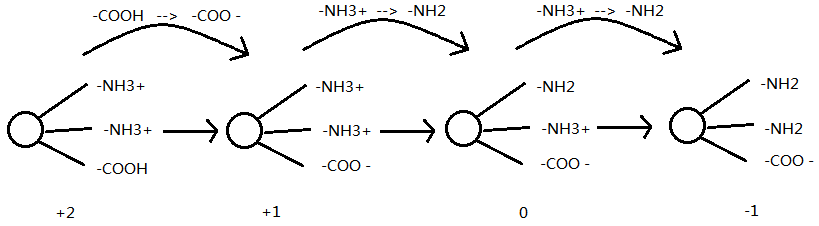
如上图所示,等电点前后分别为两个氨基的质子的丢失,因此区两个氨基的pK值相加除以2即可。
[1]:必需氨基酸共有10种:Lys、Trp、Phe、Met、Thr、Ile、Leu、Val、Arg和His。人体虽能够合成Arg和His,但合成的量通常不能满足正常的需要,因此这两种氨基酸又被称为半必需氨酸。-Tip MTV Hall